sexta-feira, 9 de dezembro de 2011
Lei de Arquimedes
Qualquer corpo quando mergulhado num líquido recebe da parte deste uma impulsão vertical, de baixo para cima, de valor igual ao peso do volume de líquido deslocado.
Porque é que a Torre de Pisa não cai, apesar de estar inclinada?
A Torre de Pisa não cai porque o seu centro de gravidade passa pela área da base de sustentação.
 |
| Torre de Pisa - Itália |
Porque é que os puxadores das portas são colocados no lado oposto às dobradiças?
Os puxadores das portas são colocados no lado oposto às dobradiças, ou seja o mais longe das dobradiças possível para aumentar o efeito de rotação da força que exercemos ao abrir ou fechar, ou seja para que se possa abrir/fechar a porta mais facilmente, sem ter que exercer tanta força.
Leis de Newton (Leis do Movimento)
1ª Lei de Newton ou Lei da Inércia
Qualquer corpo permanece em repouso ou em movimento rectilíneo uniforme enquanto as força que nele actuam têm resultante nula.
(FR=0)

(Centro da Terra)
N = P
N - Força Normal - é sempre perpendicular à superfície
P - Peso
P - N = FR = 0N
Inércia - é a resistência que o corpo oferece à alteração do seu estado de repouso ou movimento rectilíneo uniforme.
_________________________________________________________________________
2ª Lei de Newton ou Lei Fundamental da Dinâmica
A força resultante do conjunto das forças que actuam num corpo produz nele uma aceleração com a mesma direcção e o mesmo sentido da força resultante, que é tanto maior quanto maior for a intensidade da força resultante.
(FR= m x a - força resultante = massa x aceleração)
Para dois corpos com a mesma massa:
>FR - > Aceleração que o corpo adquire
ou
< FR - <a
(Grandezas directamente proporcionais)
Para dois corpos com a mesma força resultante:
>mcorpo - <a
ou
<mcorpo - >a
(Grandezas inversamente proporcionais)
Para dois corpos com a mesma aceleração:
>mcorpo - >FR
ou
<mcorpo-< FR
(Grandezas directamente proporcionais)
FR = mcorpo x a
mcorpo = FR/a
a = FR/mcorpo
Caso particular da 2ª Lei de Newton
P = m x g
g - aceleração gravítica = 9,8
P - peso
_________________________________________________________________________
3ª Lei de Newton ou Lei da Acção-Reacção
Quando dois corpo interagem, à acção de um corpo sobre o outro corresponde sempre uma reacção igual e oposta que o segundo corpo exerce sobre o primeiro.
As forças actuam sempre aos pares.
As forças acção-reacção encontram-se aplicadas em corpos diferentes.
Não se calcula FR no par acção-reacção.
Aceleração Média
am = Δv / Δt = vf – vi / tf - ti
Acelaração Média no S.I.: m/s2 (metros por segundo ao quadrado) - significa que em cada segundo o corpo aumenta a sua velocidade x metros por segundo
Rapidez Média
rm = distância percorrida / intervalo de tempo = d / Δt
Rapidez Média no S.I.: m/s (metros por segundo)
Deslocamento (Δx)
Deslocamento (Δx) - mudança da posição de um corpo para outra posição, ou seja, diferença entre a posição final e inicial, que o corpo ocupa ao longo do tempo.
- é uma grandeza vectorial.
Δx = xf - xi
- é uma grandeza vectorial.
Δx = xf - xi
A distância é igual ao deslocamento quando o movimento é rectilíneo sem inversão de sentido
Revisões
7º Ano - "Terra no Espaço"
Superenxame » Enxame » Galáxia » Sistema » Planeta
ex: Local ou Virgem » Grupo Local » Via Láctea » Sistema Solar » Terra
Órbita/Trajectória:
Superenxame » Enxame » Galáxia » Sistema » Planeta
ex: Local ou Virgem » Grupo Local » Via Láctea » Sistema Solar » Terra
 |
| Figura 1 - Movimento de Rotação e Translação da Terra |
- Linha imaginária que une as diferentes posições que o corpo ocupa no seu movimento.
- Tipos:
- Rectilínea - se o corpo descrever o movimento rectilíneo;
- Curvilíneo - se o corpo descrever o movimento curvilíneo.
8º Ano
Estamos em movimento ou em repouso?
Depende do referencial (objecto do qual se observa)
Diz-se que os conceitos de movimento e repouso são relativos porque depende do referencial.
Movimento de um corpo - alteração da posição do corpo, em relação a um determinado referencial, ao longo do tempo;
Repouso de um corpo - não há alteração da posição do corpo em relação a um determinado referencial, ao longo do tempo.
quinta-feira, 16 de junho de 2011
Visita de Estudo à ETAR de Beirolas
No dia 16 de Junho de 2010 realizámos uma visita de estudo à ETAR (Estação de Tratamento de Águas Residuais) de Beirolas (Figura 1).
Saímos da escola às nove e meia e começamos a caminhada. Quando chegámos à ETAR fomos levados para um auditório onde vimos um filme que introduzia a ETAR, as fases do tratamento da água, os equipamentos utilizados...
Depois de vermos o filme fomos ver o resto da Estação.
Começámos por ver a entrada do esgoto na ETAR, e depois a fase seguinte, o Pré- -Tratamento, no qual são retirados os sólidos maiores através de grades, e areias. Nesta fase são ainda retiradas as gorduras existentes na água, o que é retirado nesta fase é depois levado para aterros sanitários.
A fase seguinte é designada de Decantação Primária, no qual é utilizada a técnica da sedimentação, os compostos da água mais densos vão para o fundo e os menos densos flutuam, sendo depois removidos por uma ponte com uns ferros que raspam o chão e tiram os compostos a flutuar (Figura 2). As lamas são depois tratadas, parte delas são aproveitadas na produção de energia elécrica (Biogás), e outra parte é utilizada na produção de fertelizantes para a agricultura.
Depois fomos ver o Tratamento Biológico, que serve para eliminar qualquer matéria orgânica ainda existente através de microrganismos aeróbicos (nessecitam de oxigénio) sendo necessário o arrejamento da água com oxigénio através de chuveiros colocados no fundo dos tanques. Estes microrganismos alimente-se da poluição da água, depois crescem e formam uma papa que tem que depois ser retirada, esta papa é depois misturada com as outras lamas.
Depois vimos a Decantação Secundária na qual há a sedimentação do floco biológico da água em tratamento. No final desta fase a água já tem uma core muito mais transparente.
Depois a água é filtrada para retirar qualquer resíduo que ainda reste. No final são utilizadas luzes ultra-violetas para eliminar microrganismos perigosos para a saúde humana, depois a água é devolvida ao rio.
Para a inexistência de maus cheiros a maior parte dos processos é feita dentro de um armazém e depois o ar é "aspirado" e levado através de condutas até à Desodorização, onde são feitas várias reacções químicas para tirar o mau cheiro.
A função das ETAR é limpar a água utilizada pelos humanos e depois devolver aos rios (ao seu ponto de origem). O caudal da água a entrar na ETAR vai variando conforme a altura do dia, de manhã, por causa do pequeno almoço, e do duche, as horas das refeições...
 |
| Figura 1 |
Saímos da escola às nove e meia e começamos a caminhada. Quando chegámos à ETAR fomos levados para um auditório onde vimos um filme que introduzia a ETAR, as fases do tratamento da água, os equipamentos utilizados...
Depois de vermos o filme fomos ver o resto da Estação.
Começámos por ver a entrada do esgoto na ETAR, e depois a fase seguinte, o Pré- -Tratamento, no qual são retirados os sólidos maiores através de grades, e areias. Nesta fase são ainda retiradas as gorduras existentes na água, o que é retirado nesta fase é depois levado para aterros sanitários.
A fase seguinte é designada de Decantação Primária, no qual é utilizada a técnica da sedimentação, os compostos da água mais densos vão para o fundo e os menos densos flutuam, sendo depois removidos por uma ponte com uns ferros que raspam o chão e tiram os compostos a flutuar (Figura 2). As lamas são depois tratadas, parte delas são aproveitadas na produção de energia elécrica (Biogás), e outra parte é utilizada na produção de fertelizantes para a agricultura.
 |
| Figura 2 |
Depois fomos ver o Tratamento Biológico, que serve para eliminar qualquer matéria orgânica ainda existente através de microrganismos aeróbicos (nessecitam de oxigénio) sendo necessário o arrejamento da água com oxigénio através de chuveiros colocados no fundo dos tanques. Estes microrganismos alimente-se da poluição da água, depois crescem e formam uma papa que tem que depois ser retirada, esta papa é depois misturada com as outras lamas.
Depois vimos a Decantação Secundária na qual há a sedimentação do floco biológico da água em tratamento. No final desta fase a água já tem uma core muito mais transparente.
Depois a água é filtrada para retirar qualquer resíduo que ainda reste. No final são utilizadas luzes ultra-violetas para eliminar microrganismos perigosos para a saúde humana, depois a água é devolvida ao rio.
Para a inexistência de maus cheiros a maior parte dos processos é feita dentro de um armazém e depois o ar é "aspirado" e levado através de condutas até à Desodorização, onde são feitas várias reacções químicas para tirar o mau cheiro.
A função das ETAR é limpar a água utilizada pelos humanos e depois devolver aos rios (ao seu ponto de origem). O caudal da água a entrar na ETAR vai variando conforme a altura do dia, de manhã, por causa do pequeno almoço, e do duche, as horas das refeições...
segunda-feira, 6 de junho de 2011
Luz
Porque vemos os objectos?
Os nossos olhos vêem os objectos porque estes emitem ou reflectem luz visível.
Classificação dos objectos quanto à passagem da LUZ:
- Opacos (Figura 1);
- Translucido (deixam passar parcialmente a LUZ) (Figura 2);
- Transparentes (Figura 3).
 |
| Figura 1 |
 |
| Figura 2 |
 |
| Figura 3 |
Triângulo da Visão (Figura 4)
 |
| Figura 4 |
Porque razão vemos a nossa imagem num espelho e não a vemos numa parede?
Porque no espelho temos um superfície lisa e polida, enquanto que numa parede temos uma superfície rugosa.
Numa superfície lisa e polida ocorre a Reflexão Regular (Figura 5), enquanto que na superfície rugosa ocorre a Reflexão Irregular ou Difusão (Figura 6).
| Figura 5 |
 |
| Figura 6 |
Espelhos:
Existem diferentes tipos de espelhos:
- Espelho plano: imagem direita, forma-se à mesma distância, que do objecto ao espelho;
- Espelho côncavo: imagem invertida, ampliada;
- Espelho convexo: imagem direita, menor que o objecto.
Som
Propriedades do SOM
- Altura do Som:
- Agudo, Fino ou Alto;
- Grave, Grosso ou Baixo.
- Intensidade do Som:
- Forte;
- Fraco.
Relação das Propriedades do SOM com as Propriedades das Ondas
- A altura do som relaciona-se com a frequência da onda;
- A intensidade do som relaciona-se com a amplitude da onda.
O que permite distinguir a mesma nota, tocada com igual intensidade, em instrumentos diferentes é o TIMBRE.
ECO - ouvir perfeitamente o som emitido (Figura 1).
Distância mínima para que ocorra o eco é 17 metros
Ocorre quando o SOM bate num meio material e volta para trás.
REVERBERAÇÃO - sensação de prolongação do som (Figura 2).
Ocorre quando o SOM bate num meio material e novamente noutro, e assim sussecivamente.
- Altura do Som:
- Agudo, Fino ou Alto;
- Grave, Grosso ou Baixo.
- Intensidade do Som:
- Forte;
- Fraco.
Relação das Propriedades do SOM com as Propriedades das Ondas
- A altura do som relaciona-se com a frequência da onda;
- A intensidade do som relaciona-se com a amplitude da onda.
O que permite distinguir a mesma nota, tocada com igual intensidade, em instrumentos diferentes é o TIMBRE.
ECO - ouvir perfeitamente o som emitido (Figura 1).
 |
| Figura 1 |
Distância mínima para que ocorra o eco é 17 metros
Ocorre quando o SOM bate num meio material e volta para trás.
REVERBERAÇÃO - sensação de prolongação do som (Figura 2).
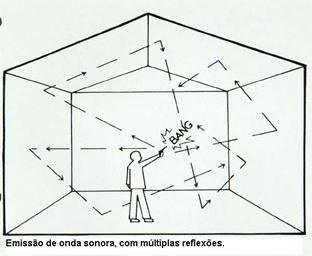 |
| Figura 2 |
Ocorre quando o SOM bate num meio material e novamente noutro, e assim sussecivamente.
domingo, 5 de junho de 2011
Ondas
O que é uma ONDA?
- É uma perturbação
- Há transferência de energia do ponto que sofreu a perturbação para outro ponto
Classificação das ONDAS:
- Mecânicas - necessitam de um meio material para se propagarem;
ex: ondas sonoras, ondas na água, ondas sísmica...
- Electromagnéticas - não precisam de um meio para se propagarem;
ex: ondas luminosas...
- Longitudinais - a direcção da perturbação coincide com a direcção da propagação da onda;
ex: onda sonora...
- Transversais - a direcção da perturbação e da propagação é perpendicular.
ex: onda luminosa...
Representação Gráfica de uma ONDA
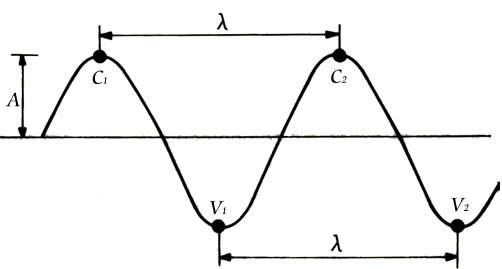 |
| Figura 1 |
Legenda (Figura 1):
- A - amplitude (m);
 (lambeda) - comprimento da onda (m);
(lambeda) - comprimento da onda (m);- T - período - tempo que a onda demora a percorrer um ciclo (m/s);
- f - frequência - número de ciclos que ocorrem numa unidade de tempo - um segundo (s-1 ou Hz).
Como é que se produzem as ONDAS?
As ONDAS produzem-se através da vibração dos corpos.
sábado, 26 de março de 2011
Como se transfere energia sob a forma de calor?
Há três processos:
- nos sólidos - condução térmica - a energia é transferida partícula a partícula, não há deslocamento (transporte) de matéria - há bons e maus condutores térmicos: exemplo de um bom condutor térmico (é mais fácil e rápida a transferência de calor): metal; exemplos de maus condutores térmicos (é difícil a transferência de calor): madeira, borracha;
- nos líquidos e gases - convecção térmica - através de correntes de convecção (apresentação 1). Há transferência de energia com deslocamento de energia (transporte) de matéria.
 |
| Apresentação 1 |
- radiação - não é necessário nenhum meio natural, e à transferência de calor através de ondas electromagnéticas.
Actividade Experimental - "TEMPERATURA / CALOR"
O QUE ACONTECE QUANDO SE COLOCAM EM CONTACTO CORPOS A DIFERENTES TEMPERATURAS?
Material:
Material:
- 2 Termómetros;
- Gobelé pequeno com 100mL de água aquecida (67ºC);
- Gobelé grande com 100mL de água à temperatura ambiente (19ºC);
- 1 Cronómetro.
Procedimento:
- Mede-se a temperatura inicial da água de ambos os gobelés;
- Coloca-se o gobelé mais pequeno dentro do gobelé maior;
- Regista-se a temperatura de ambos os gobelés de minuto a minuto.
Lista de Observações (Gobelé Pequeno/gobelé Grande):
- 1 minuto - 56ºC/24ºC;
- 2 minutos - 46ºC/32ºC;
- 3 minutos - 45ºC/35ºC;
- 4 minutos - 43,5ºC/38ºC;
- 5 minutos - 42,5ºC/38ºC;
- 6 minutos - 41ºC/37ºC;
- 7 minutos - 40ºC/37,5ºC;
- 8 minutos - 39,5ºC/37ºC;
- 9 minutos - 39ºC/37ºC;
- 10 minutos - 38,5ºC/37ºC;
- 11 minutos - 38ºC/37,5ºC;
- 12 minutos - 37,5ºC/36ºC;
- 13 minutos - 37ºC/36ºC;
- 14 minutos - 37ºC/35ºC;
- 15 minutos - 36,5ºC/35ºC;
- 16 minutos - 36ºC/35ºC;
- 17 minutos - 35,5ºC/35ºC;
- 18 minutos - 35,5ºC/34,5ºC;
- 19 minutos - 35ºC/34ºC;
- 20 minutos - 35ºC/34ºC;
- 21 minutos - 34,5ºC/33,5ºC;
- 22 minutos - 34ºC/33ºC;
- 23 minutos - 33,5ºC/33ºC;
- 24 minutos - 33,5ºC/33ºC;
- 25 minutos - 33ºC/33ºC - EQUILIBRIO TÉRMICO.
Conclusão:
A temperatura da água do gobelé pequeno (água aquecida) desceu, e a temperatura água do gobelé grande (água à temperatura ambiente) aumentou até se dar o equilíbrio térmico - ambas as temperaturas são iguais.
Nesta experiência:
- a fonte: gobelé com água aquecida;
- o receptor: gobelé com água à temperatura ambiente;
Distinção de Calor e Temperatura:
- Calor- é a transferência de energia térmica entre dois corpos em contacto a diferentes temperaturas - do corpo mais quente para o mais frio;
- Temperatura - é uma grandeza física que se relaciona com o grau de agitação dos corpúsculos e com a energia cinética média dos corpúsculos.
quarta-feira, 23 de fevereiro de 2011
Energia
O que é?:
Energia Dissipada + Energia Útil = Energia Fornecida
- É uma grandeza física, não vectorial;
- Não é uma substância;
- Não é uma força;
- Manifesta-se sob diferentes formas:
- energia sonora;
- energia luminosa (luz visível);
- energia potencial química;
- energia mecânica;
- energia eléctrica,
- energia radiante;
- energia térmica.
- Transforma-se;
- Existem várias fontes de energia:
- renováveis: Sol,
vento, água, biomassa;
vento, água, biomassa;
- não renováveis: combustíveis fosseis, combustíveis nucleares.
As duas formas fundamentais da Energia:
- Energia Cinética (Ec= 1/2m.v2): energia associada ao movimento;
- Energia Potencial (existem vários tipos: Energia Potencial Gravítica (Epg= m.g.h), Energia Potencial Química, Energia Potencial Elástica): energia que se encontra armazenada e pode vir a ser utilizada.
Nome: | Representação: |
Energia Total | Et |
Energia Potencial Gravítica | Epg |
Energia Cinética | Ec |
Et=Epg+ Ec ---> Princípio da Conservação da Energia: a energia é constante, num sistema físico.
- A Energia Eléctrica tem como objectivo a transformação em Energia Luminosa (energia útil: energia utilizada para o fim a que se destina);
- A Energia Eléctrica é também transformada em Energia Térmica (energia secundária que não é produzida para o fim a que se destina: energia dissipada).
Corpúsculos
Teoria cinético-corpuscular: toda a matéria é constituída por corpúsculos. A matéria é descontinua: existem espaços vazios entre os corpúsculos.
Os corpúsculos encontram-se em constante movimento. Aumentando a temperatura, a rapidez dos movimentos dos corpúsculos aumenta.
aumentando a
temperatura
sólido ---> líquido a agitação dos corpúsculos aumenta, os espaços vazios aumentam, forças de coesão são mais fracas e a organização diminui
Os corpúsculos encontram-se em constante movimento. Aumentando a temperatura, a rapidez dos movimentos dos corpúsculos aumenta.
aumentando a
temperatura
sólido ---> líquido a agitação dos corpúsculos aumenta, os espaços vazios aumentam, forças de coesão são mais fracas e a organização diminui
 |
Iões
Composto iónico: são substâncias constituídas por iões positivos (catiões) e por iões negativos (aniões).
O que são iões?: são partículas com carga eléctrica, formadas de átomos (ou conjunto de átomos) que receberam ou perderam electrões.
Átomo de Cloro:
Cl + 1e- ião cloreto: ião negativo ou anião
e-: electrão (partícula negativa)
O composto iónico sólido é sempre neutro.
Existem regras para a representação Simbólica dos Iões:
Existem também regras de escrita das fórmulas químicas dos iões, elas são:
O que são iões?: são partículas com carga eléctrica, formadas de átomos (ou conjunto de átomos) que receberam ou perderam electrões.
Átomo de Cloro:
Cl + 1e- ião cloreto: ião negativo ou anião
e-: electrão (partícula negativa)
O composto iónico sólido é sempre neutro.
Existem regras para a representação Simbólica dos Iões:
- Para um ião positivo (Catião) coloca-se como “expoente” no símbolo do elemento o sinal “+”.
- Para um ião negativo (Anião) coloca-se como “expoente” no símbolo do elemento o sinal “-“.
- Se o ião tiver mais do que uma carga positiva ou negativa, coloca-se no expoente, antes do sinalo número de cargas.
- Os iões também podem ser formados por mais do que um átomo de elementos diferentes, iões poliatómicos.
Existem também regras de escrita das fórmulas químicas dos iões, elas são:
- Na fórmula química do composto iónico escreve-se primeiro o símbolo do ião positivo e depois o símbolo do ião negativo;
- Na leitura do nome do composto iónico, lê-se primeiro o nome do ião negativo e depois o nome do ião positivo;
- O número de cargas positivas é igual ao número de cargas negativas.
Lei de Lavoisier
Frase da Lei de Lavoisier: "Na Natureza nada se perde, nada se ganha, tudo se transforma"
Seguindo esta frase percebemos que numa reacção química o massa total dos reagentes e igual à massa total dos produtos de reacção, nalguns casos tendo que recorrer a um acerto das equações químicas. Este acerto é feito acrescentando o número que pretendemos multiplicar pelo número de átomos que queremos acertar (ao seja coloca-se o número atrás da fórmula química. NOTA: O número influência toda a fórmula química).
Exemplo:
metano (g) + oxigénio (g) --> dióxido de carbono (g) + água (g)
Equação química: CH4 (g) + O2 (g) ---> CO2 (g) + H2O (g)
Nº de átomos: 1C/4H 2O 1C/2O 2H/1O
Nº Total de átomos: 1C/4H/2O 1C/3O/2H
Equação acertada: CH4 (g) + 2O2 (g) ---> CO2 (g) + 2H2O (g)
Nº de átomos: 1C/4H 42O 1C/2O 4 2H/2 1O
Seguindo esta frase percebemos que numa reacção química o massa total dos reagentes e igual à massa total dos produtos de reacção, nalguns casos tendo que recorrer a um acerto das equações químicas. Este acerto é feito acrescentando o número que pretendemos multiplicar pelo número de átomos que queremos acertar (ao seja coloca-se o número atrás da fórmula química. NOTA: O número influência toda a fórmula química).
Exemplo:
metano (g) + oxigénio (g) --> dióxido de carbono (g) + água (g)
Equação química: CH4 (g) + O2 (g) ---> CO2 (g) + H2O (g)
Nº de átomos: 1C/4H 2O 1C/2O 2H/1O
Nº Total de átomos: 1C/4H/2O 1C/3O/2H
Equação acertada: CH4 (g) + 2O2 (g) ---> CO2 (g) + 2H2O (g)
Nº de átomos: 1C/4H 4
Subscrever:
Mensagens (Atom)
